![]() Franck Mouthon, Président-Directeur Général et co-fondateur de Theranexus commente : « Au cours de ce semestre, Theranexus a poursuivi le développement et l’enrichissement de son portefeuille de candidats médicaments. Nous sommes impatients de partager les résultats cliniques de phase 1 de notre candidat-médicament THN201 dans la maladie d’Alzheimer fin 2019 et de phase 2 de notre candidat-médicament THN102 dans la maladie de Parkinson au 1er trimestre 2020. Ce premier semestre a également été marqué par la signature d’un accord de principe avec la « Beyond Batten Disease Foundation » (BBDF) pour le développement et la commercialisation du candidat médicament BBDF 101 dans la maladie de Batten. Ces nombreux développements ont été accompagnés d’une gestion rigoureuse des dépenses, en phase avec les ambitieux programmes cliniques de la société. »
Franck Mouthon, Président-Directeur Général et co-fondateur de Theranexus commente : « Au cours de ce semestre, Theranexus a poursuivi le développement et l’enrichissement de son portefeuille de candidats médicaments. Nous sommes impatients de partager les résultats cliniques de phase 1 de notre candidat-médicament THN201 dans la maladie d’Alzheimer fin 2019 et de phase 2 de notre candidat-médicament THN102 dans la maladie de Parkinson au 1er trimestre 2020. Ce premier semestre a également été marqué par la signature d’un accord de principe avec la « Beyond Batten Disease Foundation » (BBDF) pour le développement et la commercialisation du candidat médicament BBDF 101 dans la maladie de Batten. Ces nombreux développements ont été accompagnés d’une gestion rigoureuse des dépenses, en phase avec les ambitieux programmes cliniques de la société. »
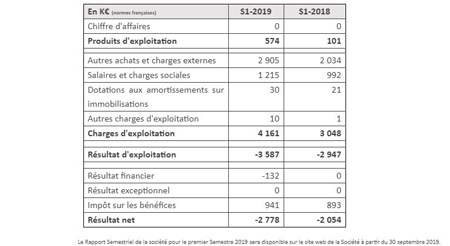
Les autres achats et charges externes sont en hausse sur le semestre à 2 905 K€ contre 2 034 K€ au premier semestre 2018. Cela est lié à la montée en puissance du programme de phase 2 dans la maladie de Parkinson et au lancement du programme de phase 1b dans la démence au cours du second semestre 2018.
La hausse des salaires et charges sociales, qui passent de 992 K€ au premier semestre 2018 à 1 215 K€ au premier semestre 2019, traduit principalement l’effet en année pleine de recrutements réalisés au cours de l’année 2018, notamment le renforcement de l’équipe recherche et développement.
En conséquence, la perte d’exploitation est passée de -2 947 K€ pour le premier semestre 2018 à -3 587 K€ pour le premier semestre 2019.
Le résultat financier est déficitaire de 132 K€ pour le premier semestre 2019 notamment en raison des intérêts financiers encourus sur les financements obtenus auprès d’établissements bancaires, mis en place au début du second semestre 2018, et de Bpifrance.
Après comptabilisation de 941 K€ de produit d’impôt, principalement du Crédit Impôt Recherche, la perte nette ressort à -2 778 K€ au premier semestre 2019 contre -2 054 K€ au premier semestre 2018.
La trésorerie au 30 juin 2019 s’élève à 10 231 K€. Ce montant ne comprend ni le fruit de la levée de fonds de 2 245 K€ réalisée début juillet 2019, ni le remboursement des crédits d’impôts à percevoir au titre de l’exercice 2018 d’un montant de 1 721 K€.
État du portefeuille de candidats médicaments en clinique, de l’activité partenariale et des principaux projets scientifiques en cours
Theranexus a annoncé le 24 septembre le recrutement du dernier patient naïf atteint de la maladie de Parkinson dans son étude clinique de phase 2 visant à évaluer la tolérance et l’efficacité de son candidat médicament THN102 (combinaison modafinil / flécaïnide) sur des symptômes non moteurs de la maladie (somnolence, troubles de l’attention et de la cognition). Cette triade qui représente un besoin médical non-satisfait important dans la pathologie, constitue un marché potentiel à très forte valeur (estimé à plus de 2 milliards de dollars). Les résultats du THN102 sont attendus au 1er trimestre 2020.
Dans la narcolepsie, l’analyse approfondie des résultats de l’étude de phase 2 a confirmé la surreprésentation de patients narcoleptiques faiblement répondeurs qui a eu pour conséquence une absence de différence d’efficacité par rapport au traitement de référence [1]. La poursuite du programme dans la narcolepsie est en attente des résultats de l’étude de Phase 2 dans la maladie de Parkinson.
Par ailleurs, la Société a annoncé l’obtention en Chine d’un brevet renforçant la couverture internationale de son candidat médicament THN102 jusqu’en 2034.
Candidat-Médicament THN201 - Fin du recrutement pour l’étude de phase 1b pour le traitement des troubles neurocognitifs dans la Maladie d’Alzheimer
La Société a annoncé le 17 septembre dernier avoir inclus le dernier sujet sain dans son étude de Phase 1b comparant l’efficacité pharmacologique de son candidat médicament THN201 avec celle du traitement de référence des troubles neurocognitifs dans la maladie d’Alzheimer. Les résultats sont attendus au 4ème trimestre 2019.
THN201 est une combinaison de donépezil, agissant sur l’activité neuronale, et de méfloquine agissant sur l’activité des cellules gliales. Au total, 152 sujets sains ont été recrutés dans 10 centres en Europe. L’étude est menée en double aveugle, randomisée, en trois groupes parallèles pour évaluer l’activité pro-cognitive, la tolérance et la pharmacocinétique de THN201 comparativement au traitement de référence seul et au placebo. Le THN201 a déjà démontré en préclinique un profil d’efficacité pharmacologique supérieur au traitement de référence de la maladie d’Alzheimer ainsi qu’un excellent profil de tolérance.
Les résultats de la phase 1 relatif à la sécurité, tolérance et pharmacocinétique chez les patients atteints de douleurs neuropathiques sont positifs et permettent à Theranexus de préparer activement une phase 2. Cet essai clinique devrait inclure 370 patients souffrant de douleurs neuropathiques d’origine diabétique ou post-zostérienne (suivant un zona) dans 40 à 45 sites d’investigation en Europe. Le critère principal de cette étude sera basé sur une autoévaluation régulière de sa douleur par le patient lui-même avec l’utilisation d’une échelle numérique.
Signature d’un partenariat de principe avec la « Beyond Batten Disease Foundation » (BBDF) pour le développement et la commercialisation du candidat médicament BBDF 101 dans la maladie de Batten
Le 27 juin 2019, la Société a signé un accord de principe (term sheet) avec l’association Beyond Batten Disease Foundation (BBDF) afin de conduire le programme de développement clinique devant permettre l’enregistrement et la commercialisation du candidat-médicament BBDF101 dans la maladie de Batten. BBDF a financé les travaux de recherche visant à identifier et à valider BBDF101 pour le traitement de la forme juvénile de la maladie de Batten. Theranexus et BBDF porteront conjointement le développement clinique du produit aux États-Unis dans une étude devant permettre son enregistrement. Theranexus disposera d’une licence exclusive mondiale pour l’exploitation commerciale du produit. Bénéficiant d’une période d’exclusivité de six mois, l’accord devrait être signé d’ici fin 2019.
Pour financer le programme de développement clinique devant permettre l’enregistrement et la commercialisation du candidat-médicament BBDF 101 dans la maladie de Batten, Theranexus a réalisé un placement réservé à une catégorie de personnes d’un montant d’environ 2,2 millions d’euros le 11 juillet dernier.
Theranexus bénéficie d’une aide de 6,2 millions d’euros dans le cadre du Programme investissement d’avenir opéré par Bpifrance, pour le Programme Neurolead. Ce programme, coordonné par Theranexus en collaboration avec le Collège de France et le CEA, a pour objectif de développer et d’industrialiser une plateforme unique d’identification et de caractérisation de candidats médicaments dans le domaine des troubles neurologiques. Dotée des dernières innovations en neurosciences et en intelligence artificielle, cette plateforme permettra de généraliser et systématiser le concept thérapeutique de Theranexus en amplifiant ses capacités d’applications thérapeutiques. L’accord de consortium devrait être signé d’ici fin 2019. A ce jour, aucune somme n’a encore été versée par Bpifrance à Theranexus et ses partenaires.
La Société a récemment annoncé la publication de deux articles scientifiques, d’une part, sur l’enrichissement de la bibliothèque propriétaire d’effecteurs de cellules gliales dans la revue scientifique « ASSAY and Drug Development Technologies », et d’autre part, sur le profil de pharmacologie clinique de THN102 dans le « British Journal of Clinical Pharmacology ».
En juin 2019, Theranexus a constitué son Conseil Scientifique composé de 4 experts de renom qui a pour mission d’assister et de conseiller la Société dans ses choix notamment dans les stratégies d’identification, de sélection et de qualification de candidats médicaments ciblant les interactions entre les deux populations cellulaires du cerveau, les neurones et les cellules gliales dans le domaine des maladies du Système Nerveux Central (SNC).
Plus globalement sur 2019, Theranexus a participé à de nombreux congrès où la Société a présenté ses résultats scientifiques sur le rôle des connexines astrogliales dans l’efficacité de THN201 dans les troubles neurocognitifs liés à la maladie d’Alzheimer [2] lors de la conférence AD/PD [3] ou encore de nouvelles données scientifiques sur les interactions neurogliales au cours du Congrès NeuroFrance et à la Conférence « Advances in Cell Based Screening in Drug Discovery » ou dernièrement sur le mécanisme d’action et l’impact du THN101 dans les douleurs neurologiques lors du Congrès Européen de la Douleur (EFIC).