 Accroître la position de leader de la France en matière de recherche clinique est essentiel à l’accès précoce pour les patients aux innovations thérapeutiques. Depuis de nombreuses années, le Leem, grâce à son enquête sur la recherche clinique, tire la sonnette d’alarme sur la baisse de compétitivité et d’attractivité de la France dans ce domaine. Malgré les actions mises en place (convention unique, mobilisation de l’ANSM, évolution des modalités de travail des CPP*), cette tendance peine à être inversée. La mobilisation exceptionnelle des différents acteurs de la recherche pendant l’épidémie de la COVID-19, a montré que la France était capable de grandes avancées. Depuis le début de l’épidémie, 77 essais thérapeutiques ont été autorisés dont 22 à promotion industrielle, résultat d’une coordination renforcée et d’un dialogue permanent entre les autorités, les promoteurs et les équipes cliniques et de recherche. Pour que la France reste une terre d’excellence de la recherche clinique et préserve ainsi sa capacité à garantir à tous l’accès aux innovations, les entreprises du médicament (Leem) appellent à inscrire cette dynamique dans le temps avec la proposition de 10 mesures clés.
Accroître la position de leader de la France en matière de recherche clinique est essentiel à l’accès précoce pour les patients aux innovations thérapeutiques. Depuis de nombreuses années, le Leem, grâce à son enquête sur la recherche clinique, tire la sonnette d’alarme sur la baisse de compétitivité et d’attractivité de la France dans ce domaine. Malgré les actions mises en place (convention unique, mobilisation de l’ANSM, évolution des modalités de travail des CPP*), cette tendance peine à être inversée. La mobilisation exceptionnelle des différents acteurs de la recherche pendant l’épidémie de la COVID-19, a montré que la France était capable de grandes avancées. Depuis le début de l’épidémie, 77 essais thérapeutiques ont été autorisés dont 22 à promotion industrielle, résultat d’une coordination renforcée et d’un dialogue permanent entre les autorités, les promoteurs et les équipes cliniques et de recherche. Pour que la France reste une terre d’excellence de la recherche clinique et préserve ainsi sa capacité à garantir à tous l’accès aux innovations, les entreprises du médicament (Leem) appellent à inscrire cette dynamique dans le temps avec la proposition de 10 mesures clés.
Quelle position tient la France en termes de recherche clinique au niveau mondial ? Afin de répondre à cette question, le leem réalise tous les deux ans une enquête qui permet de suivre l’évolution de plusieurs indicateurs sur les essais cliniques. Cette 10ème édition analyse les données renseignées dans la base gouvernementale américaine (clinicaltrials.gov) et celle du Leem (OSCAR) concernant les essais initiés dans le monde par les entreprises du médicament sur la période 2018-2019. Un total de 5 819 essais initiés par les entreprises du médicament a ainsi pu être pris en compte ainsi qu’un échantillon de 378 essais pour lesquels la mise en œuvre sur le territoire a spécifiquement été analysée.
Dans sa participation aux essais mondiaux, la France reste au 1er semestre 2019 au 4ème rang européen derrière l’Allemagne, le Royaume-Uni et l’Espagne. L’ensemble des pays européens participent moins aux essais précoces (phases 1 et 1/2) que les seuls Etats-Unis (33 % vs 47 %) et la France n’occupe que le 5ème rang européen (5 %) derrière le Royaume-Uni (10 %), l’Allemagne (8 %), la Belgique (6 %) et l’Espagne (6 %).
Point positif, la France conserve son 2ème rang européen en oncologie avec une participation à 19 % des essais cliniques mondiaux, derrière l’Espagne (22 %).
Entre 2018 et 2019, sur l’ensemble des essais conduits dans l’un des pays du « top 3 » européen, 956 essais n’ont pas associé la France. Il s’agit principalement d’essais de phases précoces conduits essentiellement par des biotechs, qui ont préféré l’un de ces trois pays à la France pour initier leurs essais.
L’analyse des données de la base OSCAR, montre que 46 % des essais concernent l’oncologie, 12 % les maladies rares, 7 % les Médicaments de Thérapie Innovantes (MTI) et 6 % la pédiatrie.
« Les essais cliniques sont indispensables pour un accès précoce des patients aux innovations. Ils le sont également pour le maintien de l’expertise des professionnels de santé et l’excellence du pays en matière de recherche. La France doit être plus attractive au niveau international pour attirer les essais cliniques, en particulier dans les phases précoces du développement », explique Christian Deleuze, Président de la Commission Recherche & Innovation du Leem.
Entre 2018 et 2019, les temps d’initiation des essais cliniques ont diminué :
![]() De 59 à 41 jours pour l’autorisation par l’ANSM
De 59 à 41 jours pour l’autorisation par l’ANSM
![]() De 89 à 76 jours pour l’avis éthique par le CPP
De 89 à 76 jours pour l’avis éthique par le CPP
![]() De 76 à 70 jours pour la signature de la convention unique.
De 76 à 70 jours pour la signature de la convention unique.
L’articulation entre ces trois étapes génère encore des délais importants et ceci alors que le cadre réglementaire français permet de les réaliser en parallèle.
Autre point à améliorer : les étapes de mise en place des centres investigateurs puis de recrutement du 1er patient dans l’essai qui sont réalisées en 77 jours (contre 72 jours dans l’enquête précédente)
Au total, 204 jours sont nécessaires entre la première démarche administrative et l’inclusion d’un 1er patient dans un essai clinique en France. Ce délai doit être optimisé puisqu’il est de 189 jours en Espagne et de 139 jours, en prenant en compte chaque 1er patient inclus, à l’échelle de l’Europe.
La pandémie a engendré une recherche menée de manière urgente et massive. De nombreux pays ont rapidement développé des projets pour caractériser le nouveau virus et sa physiopathologie, développer un traitement spécifique ou un vaccin, évaluer le repositionnement de médicaments dans de nouvelles indications. Ces projets sont portés par des académiques, des industriels ou des consortia public-privé. Début août à travers le monde, plus de 2 800 études étaient recensées dans clinicaltrials.gov avec près de 1 570 essais cliniques.
La France s’est fortement mobilisée et se positionne depuis avril au 2ème rang mondial en matière d’essais cliniques COVID-19 derrière les Etats-Unis. La mobilisation des équipes de recherche et des promoteurs académiques ou industriels a permis d’élaborer de nombreux protocoles de recherche à visée thérapeutique (98 essais cliniques).
Les autorités ont mis en place des procédures accélérées pour l’évaluation initiale des projets sur la prise en charge des patients atteints de la COVID-19. La dynamique impulsée a permis à l’ANSM et aux CPP d’autoriser des études cliniques sur le territoire en quelques jours. Tout a été mis en œuvre pour accélérer et alléger les procédures sans sacrifier à la qualité de l’évaluation (mobilisation de l’ensemble des acteurs, réunions dématérialisées, utilisation de la signature électronique…) et ainsi rapidement inclure les premiers patients dans les essais : certains essais ont ainsi pu débuter en 3 semaines.
Le dialogue établi entre les autorités, les promoteurs des essais et les équipes de recherche a notamment permis d’adapter régulièrement les recommandations nationales et européennes au fur et à mesure des retours d’expérience.
Adapter ces modalités de travail « inédites » à un cadre pérenne pour améliorer l’accès à la recherche clinique pourrait permettre à la France de reprendre un rôle de premier plan à l’international.
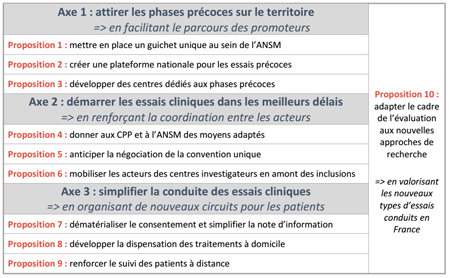
Dans un objectif de garantir l’accès aux innovations thérapeutiques pour tous et de renforcer l’attractivité de la France pour les essais cliniques, les entreprises du médicament proposent un plan en 10 propositions fondé sur les résultats de la 10ème enquête sur les essais cliniques et sur les enseignements de la pandémie COVID-19.
« La France a prouvé sa capacité à se mobiliser et à fédérer les équipes de recherche, les promoteurs et les autorités. Il faut surfer sur cette dynamique afin de réaffirmer une volonté politique forte et mettre la recherche clinique au cœur de notre souveraineté sanitaire » conclut Frédéric Collet, Président du Leem.